《浙江省瑞安市高中化學 專題2 從海水中獲得的化學物質 2.2.2 碳酸鈉的性質與應用課件 蘇教版必修1.ppt》由會員分享�����,可在線閱讀�,更多相關《浙江省瑞安市高中化學 專題2 從海水中獲得的化學物質 2.2.2 碳酸鈉的性質與應用課件 蘇教版必修1.ppt(30頁珍藏版)》請在裝配圖網上搜索。
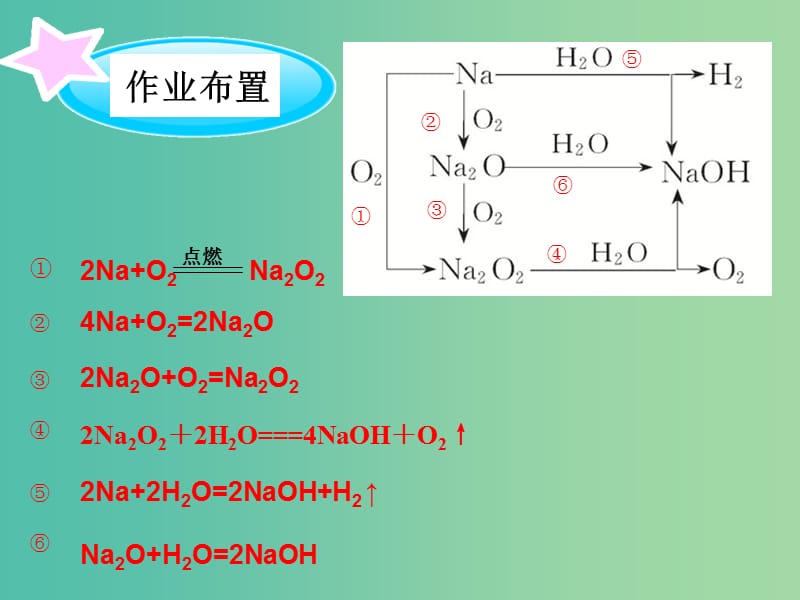
1��、,作業(yè)布置,,,,,,,,,,4Na+O2=2Na2O,,2Na2O+O2=Na2O2,,2Na2O22H2O===4NaOHO2,,2Na+2H2O=2NaOH+H2,,Na2O+H2O=2NaOH,,,,,俗名:,純堿或蘇打,一���、碳酸鈉:,化學式:,Na2CO3,,所屬的類別����?,俗名:,小蘇打,二����、碳酸氫鈉:,化學式:,NaHCO3,,鹽���,鈉鹽,所屬的類別?,白色固體,白色固體,比較容易溶于水,比較易溶于水,同等溫度下����,SNa2CO3SNaHCO3(S表示溶解度),物理性質,,,,實驗1:在兩支有Na2CO3和NaHCO3溶液的潔凈試管中分別用相同的速度加入1mLHCl溶液,觀察產生現象現
2�����、象�����。,NaHCO3��、Na2CO3均能與鹽酸反應放出CO2�����,NaHCO3反應更劇烈�,產生CO2的速率更快,現象分析:,Na2CO3與酸反應過程:,Na2CO3+HCl====NaHCO3+NaCl,總:Na2CO3+2HCl====CO2+H2O+2NaCl,NaHCO3+HCl====CO2+H2O+NaCl,氣球鼓起來了,有氣體產生���,裝有碳酸氫鈉的氣球膨脹的速度更加的快���。,現象:,實驗結論:,,1����、往裝有碳酸鈉溶液和碳酸氫鈉溶液的試管中加入2-3ml澄清的石灰水,實驗現象:,都產生白色沉淀,化學方程式:,Ca(OH)2Na2CO3===CaCO32NaOH,【實驗2】,Ca(OH)2NaHC
3�、O3===CaCO3NaOH+H2O,2、向裝有碳酸鈉溶液和碳酸氫鈉的試管中分別滴加氯化鈣溶液,觀察實驗現象����。,,【實驗3】,實驗現象:,化學方程式:,試管產生白色沉淀,試管無現象,CaCl2Na2CO3===CaCO32NaCl,1��、碳酸鈉會與KOH和KCl反應嗎�?2、碳酸鈉會與哪類物質反應����?反應具備怎樣的特征?,化學方程式:,,Na2CO3+Ca(OH)2====CaCO3+2NaOHNa2CO3+CaCl2====CaCO3+2NaCl,思考:,1.碳酸鈉會與某些堿和某些鹽反應,化學性質,鋇鹽����、鈣鹽、Ca(OH)2Ba(OH)2,酸�����、酸性氧化物,可產生沉淀、或氣體的物質,用PH試紙測定碳
4�����、酸鈉和碳酸氫鈉溶液PH,現象:,PH試紙變藍,結論:,用熱碳酸鈉溶液洗滌銅片表面的油污,現象:,油污被去除,水溶液都呈堿性�,,【實驗4】,【實驗5】,物質的量濃度相等時,Na2CO3堿性比NaHCO3更強些,應用:,除油污,在兩只干燥試管里分別放入少量Na2CO3和NaHCO3固體�����,連接好裝置�����,使導管末端伸入澄清石灰水中�����,加熱�����,觀察現象����。,實驗結論:,Na2CO3很穩(wěn)定,NaHCO3不穩(wěn)定會受熱分解,,實驗現象:裝碳酸鈉固體的裝置中澄清石灰水不變混濁����,裝碳酸氫鈉的裝置中澄清石灰水變混濁,,,滴加酚酞的碳酸鈉溶液顏色變淡,碳酸鈉與碳酸氫鈉(俗稱小蘇打)的相互轉化,碳酸氫鈉固體,一、碳酸鈉性質,1
5�����、除去下列物質中的少量雜質,1)Na2CO3固體中混有NaHCO3��,方法是反應方程式是_______,2)NaHCO3溶液中混有Na2CO3����,方法是反應方程式是___________,3)NaCl溶液中混有Na2CO3,方法是反應方程式是____________________________________,Na2CO3+CO2+H2O====2NaHCO3,Na2CO3+2HCl====2NaCl+CO2+H2O,隨堂測試,2�、除去碳酸鈉固體中含有少量的碳酸氫鈉的方法是()A、加熱B����、加入生石灰并加熱C、將固體配成溶液并通入CO2D��、加入鹽酸,A,3.欲除去碳酸氫鈉溶液中少量碳酸鈉的雜質�,適
6����、宜加入的物質是()A����、Ca(OH)2B、Ca(HCO3)2C���、鹽酸D��、CO2,D,4.下列物質露置在空氣中�,不能吸收CO2的是()A.Na2CO3B.NaOHC.NaHCO3D.Na2O,A,1.作業(yè)本,,作業(yè)布置,Na2CO3和NaHCO3的實驗探究1�、溶解度是否一樣?2���、熱穩(wěn)定性有何不同�����?3��、相同濃度溶液的PH值是否相同���?4、能否與酸反應�����?5�����、能否與堿反應�?6、能否與氯化鈣反應����?,SNa2CO3SNaHCO3,,,穩(wěn)定性:Na2CO3NaHCO3,,堿性:Na2CO3NaHCO3,,NaHCO3+HCl====CO2+H2O+NaCl,,2NaHCO3Ca(OH)2====Na2CO3Ca
7、CO3+2H2O,Na2CO3+CaCl2====CaCO3+2NaCl,NaHCO3+CaCl2,,,,實驗一:用pH試紙分別測定同濃度Na2CO3����、NaHCO3溶液的pH。,實驗結論:物質的量濃度相同時�,堿性強的是碳酸鈉。,實驗四:在兩支潔凈的試管中分別加入12mLCa(OH)2溶液��,再分別加入Na2CO3和NaHCO3溶液���,觀察現象����。,實驗結論:,NaHCO3、Na2CO3均能與Ca(OH)2反應產生白色沉淀�����,不能區(qū)別,與堿反應,Na2CO3Ca(OH)2====2NaOHCaCO3,2NaHCO3Ca(OH)2====Na2CO3CaCO3+2H2O,實驗五:在兩支潔凈的試管中分別加入
8�、12mLNa2CO3和NaHCO3溶液,再分別滴入少量CaCl溶液,觀察現象�。,能與CaCl2反應產生白色沉淀的是Na2CO3,而不是NaHCO3,實驗結論:,Na2CO3+CaCl2====CaCO3+2NaCl,NaHCO3+CaCl2,與鹽反應,,根據表中提供的信息和你觀察到的現象,設計實驗方案�����,區(qū)別碳酸鈉和碳酸氫鈉固體,,重點,易溶,易溶,相同溫度下Na2CO3的溶解度大于NaHCO3,堿性,堿性,物質的量濃度相同時Na2CO3溶液的pH比NaHCO3溶液的大,穩(wěn)定,不穩(wěn)定,NaHCO3受熱分解生成Na2CO3��、H2O和CO2,反應,反應,都放出CO2氣體���,但NaHCO3與酸反應的劇烈
9�、程度強于Na2CO3,區(qū)別碳酸鈉和碳酸氫鈉固體,純堿是重要的化工原料�,有廣泛的用途。全世界純堿產量的一半被用于制造玻璃�,其余的在制肥皂、造紙、軟化硬水�����、石油精煉�、紡織和多種化學制造業(yè)中被廣泛使用���。碳酸鈉易溶于水�����,它的水溶液有堿性����,在日常生活中可以用來去掉發(fā)面團中的酸味兒����,還可以用它的水溶液來洗滌油污的碗碟、衣物等��。,碳酸鈉晶體,碳酸鈉的用途:P52,碳酸鈉又稱為蘇打(soda)�����,是白色粉末����。俗稱純堿�,屬于鹽類物質�����,因其水溶液顯弱堿性而稱純堿�����。,制玻璃,玻璃纖維,制藥,滅火劑,發(fā)酵劑,納米自凈玻璃,制皂,紡織等,紡織,造紙,【典例】將0.4gNaOH和1.06gNa2CO3混合并配成溶液���,向溶液中滴加0.1molL-1稀鹽酸�。下列圖像能正確表示加入鹽酸的體積和生成CO2的物質的量的關系的是,【思路點撥】反應情況為,【自主解答】選C�����。向NaOH和Na2CO3混合溶液中滴加鹽酸時��,HCl首先和NaOH反應生成水和氯化鈉����,當滴入0.1L時,兩者恰好反應完全;繼續(xù)滴加時����,鹽酸和Na2CO3開始反應,首先發(fā)生HCl+Na2CO3====NaHCO3+NaCl���,不放出氣體�����,當再加入0.1L時,此步反應進行完全�����;繼續(xù)滴加時���,發(fā)生反應NaHCO3+HCl====NaCl+H2O+CO2��。此時開始放出氣體�,分析圖像可知選C�����。,
 浙江省瑞安市高中化學 專題2 從海水中獲得的化學物質 2.2.2 碳酸鈉的性質與應用課件 蘇教版必修1.ppt
浙江省瑞安市高中化學 專題2 從海水中獲得的化學物質 2.2.2 碳酸鈉的性質與應用課件 蘇教版必修1.ppt