《2022年高中化學(xué) 《豐富多彩的化學(xué)物質(zhì)》教案1 蘇教版必修1》由會員分享��,可在線閱讀��,更多相關(guān)《2022年高中化學(xué) 《豐富多彩的化學(xué)物質(zhì)》教案1 蘇教版必修1(4頁珍藏版)》請在裝配圖網(wǎng)上搜索��。
1��、2022年高中化學(xué) 《豐富多彩的化學(xué)物質(zhì)》教案1 蘇教版必修1
一��、內(nèi)容分析
教材從宏觀和微觀結(jié)合的角度通過兩個方面描述了物質(zhì)的多樣性��。一是物質(zhì)因聚集狀態(tài)不同��,可以分成氣態(tài)��、液態(tài)和固態(tài)��,并明確指出:三種狀態(tài)下由于微觀結(jié)構(gòu)��、微粒的運動方式不同��,物質(zhì)所表現(xiàn)的宏觀性質(zhì)也不同��。二是物質(zhì)因分散狀態(tài)不同��,可以分成溶液��、濁液��、膠體��,其中分散質(zhì)的粒子大小有所不同��。即便是同一種分散系——溶液��,如食鹽溶液和蔗糖溶液��,它們在水中的存在形式又各不相同��,這與溶質(zhì)在水中是否電離有關(guān)��。這就初步揭示了物質(zhì)的微觀結(jié)構(gòu)是造成物質(zhì)世界豐富多彩的重要原因��。
在介紹了物質(zhì)轉(zhuǎn)化的定性關(guān)系后��,教材明確提出新的問題:物質(zhì)的研究
2��、應(yīng)關(guān)注轉(zhuǎn)化過程中的定量關(guān)系��。結(jié)合對化學(xué)反應(yīng)中實際參加反應(yīng)粒子的質(zhì)量和數(shù)量的分析��,讓學(xué)生了解“將一定數(shù)目的微觀粒子與可稱量物質(zhì)聯(lián)系起來”的物理量——物質(zhì)的量,并結(jié)合簡單的化學(xué)反應(yīng)討論了物質(zhì)的量之間的關(guān)系��,通過標(biāo)準(zhǔn)狀況下對氣體行為的描述介紹了氣體摩爾體積和計量關(guān)系的具體應(yīng)用��。
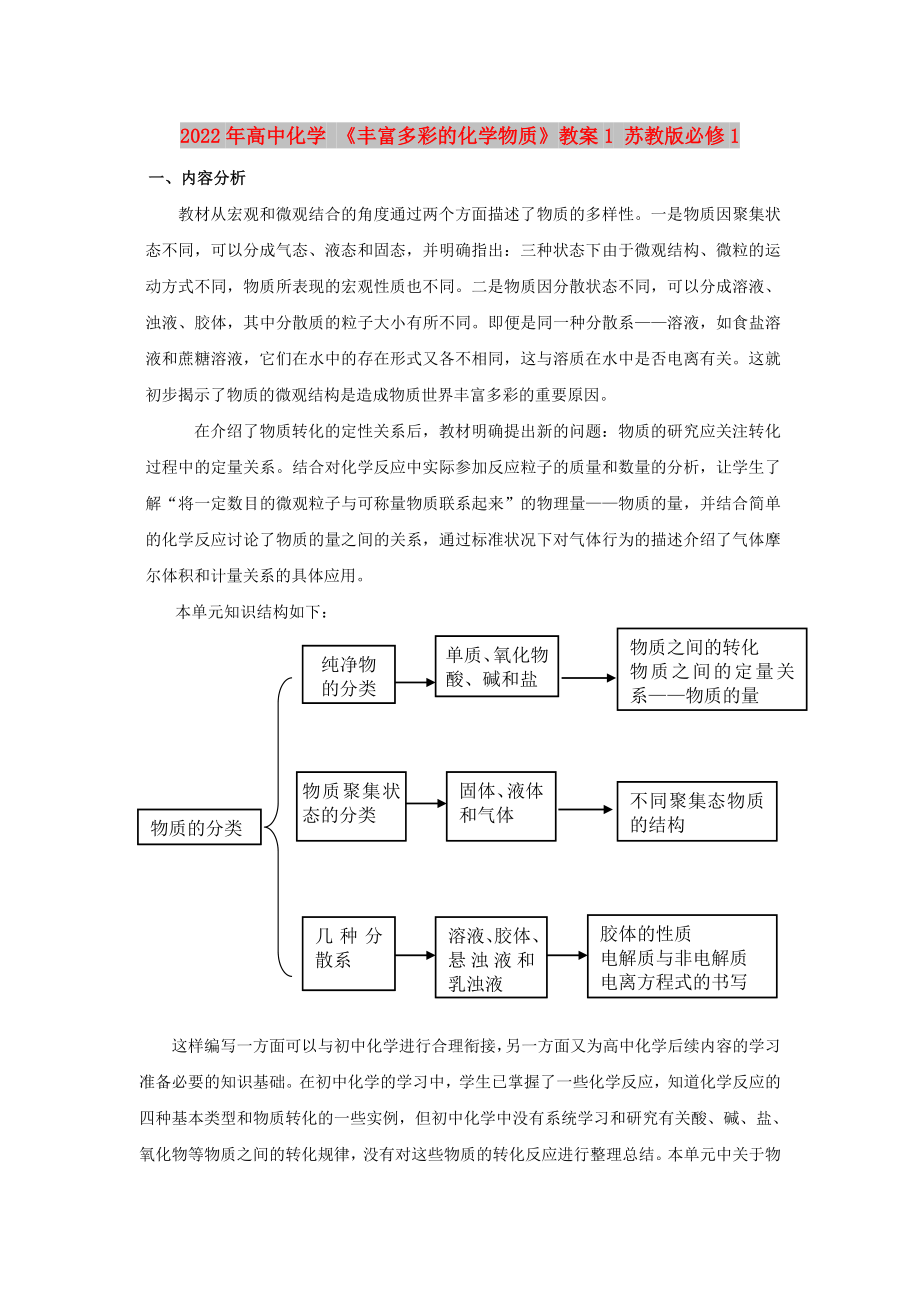
物質(zhì)之間的轉(zhuǎn)化
物質(zhì)之間的定量關(guān)系——物質(zhì)的量
本單元知識結(jié)構(gòu)如下:
單質(zhì)��、氧化物酸��、堿和鹽
純凈物的分類
固體��、液體和氣體
物質(zhì)聚集狀態(tài)的分類
不同聚集態(tài)物質(zhì)的結(jié)構(gòu)
氣體摩爾體積概念計算
物質(zhì)的分類
膠體的性質(zhì)
電解質(zhì)與非電解質(zhì)
電離方程式的書寫
溶液��、膠體��、懸濁液和
3��、乳濁液
幾種分散系
這樣編寫一方面可以與初中化學(xué)進(jìn)行合理銜接��,另一方面又為高中化學(xué)后續(xù)內(nèi)容的學(xué)習(xí)準(zhǔn)備必要的知識基礎(chǔ)��。在初中化學(xué)的學(xué)習(xí)中��,學(xué)生已掌握了一些化學(xué)反應(yīng)��,知道化學(xué)反應(yīng)的四種基本類型和物質(zhì)轉(zhuǎn)化的一些實例��,但初中化學(xué)中沒有系統(tǒng)學(xué)習(xí)和研究有關(guān)酸��、堿��、鹽��、氧化物等物質(zhì)之間的轉(zhuǎn)化規(guī)律��,沒有對這些物質(zhì)的轉(zhuǎn)化反應(yīng)進(jìn)行整理總結(jié)��。本單元中關(guān)于物質(zhì)的分類和轉(zhuǎn)化內(nèi)容正好可對初中化學(xué)中學(xué)習(xí)過的化學(xué)反應(yīng)進(jìn)行總結(jié)和歸納��,并進(jìn)行適當(dāng)?shù)耐卣购吞岣?�,幫助學(xué)生更好地認(rèn)識化學(xué)物質(zhì)��;同時��,還可以為后面學(xué)習(xí)鈉��、鎂��、氯��、氮和硫等元素化合物的性質(zhì)和轉(zhuǎn)化規(guī)律打下必要基礎(chǔ)。在初中化學(xué)的學(xué)習(xí)中��,學(xué)生已經(jīng)接觸過氣體物質(zhì)
4��、��、固體沉淀��、溶液��、濁液等具體實例��,本單元中有關(guān)“物質(zhì)的聚集狀態(tài)”��、“物質(zhì)的分散體系”的內(nèi)容就是在這個基礎(chǔ)上引導(dǎo)學(xué)生從微觀角度理解化學(xué)物質(zhì)的存在狀態(tài)��,在原有基礎(chǔ)上提升對化學(xué)物質(zhì)的認(rèn)識��,同時為后續(xù)內(nèi)容的學(xué)習(xí)準(zhǔn)備重要的基礎(chǔ)��。
教材在講完溶液��、膠體后��,緊接著安排電解質(zhì)與非電解質(zhì)的知識點��,這是不同于以往教學(xué)內(nèi)容的��。如何理解這種編排呢��?首先從教學(xué)主題——物質(zhì)世界來說��,膠體與溶液的性質(zhì)不同��,電解質(zhì)溶液與非電解質(zhì)溶液的性質(zhì)也不同��,而兩種不同都是由分散質(zhì)存在形式的差異引起的��;又正是這樣的差異��,造成物質(zhì)世界的豐富多彩性��,教師可以自然而巧妙的將兩部分知識銜接過渡��。其次��,下一專題學(xué)生將學(xué)習(xí)許多溶液中的反應(yīng)��、強(qiáng)弱電解
5��、質(zhì)概念��、離子反應(yīng)等知識。這些內(nèi)容均以電解質(zhì)和非電解質(zhì)的知識為基礎(chǔ)��,這也是專題1必須安排該內(nèi)容的原因��。在具體教學(xué)中可設(shè)計這樣的問題引導(dǎo)過渡:氯化鈉��、蔗糖溶于水都能形成溶液��,它們在水中的存在形式相同嗎��?它們存在形式的差異導(dǎo)致了其哪些性質(zhì)上的不同��?如何通過實驗證明��?
化學(xué)學(xué)科中這些知識點之間并沒有一個嚴(yán)格的因果關(guān)系��,它們也就未必存在一個認(rèn)知框架��,規(guī)定其必然的先后呈現(xiàn)順序��。專題1的組織線索較以往有較大的變化��,全新面貌的演繹需要對化學(xué)學(xué)科的理解��。那些串接一個個知識點的化學(xué)思想與內(nèi)涵��,更需要教師用心揣摩��,方能避免人為割裂本該凝為一體的知識體系��,讓學(xué)生從整體把握專題1看似紛繁的知識點背后的內(nèi)在聯(lián)系��,實現(xiàn)其
6��、學(xué)科知識的體系化��。
二��、目標(biāo)分析
《課程標(biāo)準(zhǔn)》對本部分內(nèi)容的學(xué)習(xí)提出了如下要求��。
(1)能根據(jù)物質(zhì)的組成和性質(zhì)對物質(zhì)進(jìn)行分類��。
(2)知道化學(xué)科學(xué)的主要研究對象��,知道化學(xué)是在分子層次上認(rèn)識物質(zhì)和合成新物質(zhì)的一門科學(xué)��。
(3)了解物質(zhì)的組成��、結(jié)構(gòu)和性質(zhì)的關(guān)系��;認(rèn)識化學(xué)變化的本質(zhì)��。
(4)認(rèn)識摩爾是物質(zhì)的量的基本單位,能用于進(jìn)行簡單的化學(xué)計算��,體會定量研究的方法對研究和學(xué)習(xí)化學(xué)的重要作用��。
根據(jù)《課程標(biāo)準(zhǔn)》��,在教學(xué)過程中需要達(dá)到如下目標(biāo):
(1)初步認(rèn)識物質(zhì)的科學(xué)分類方法��,學(xué)會從不同角度(尤其是物質(zhì)的組成和性質(zhì)角度)對常見物質(zhì)進(jìn)行分類��。
(2)掌握四種基本化學(xué)反應(yīng)類型��,能根據(jù)
7��、化合價的變化判斷是否為氧化還原反應(yīng)��。認(rèn)識化學(xué)反應(yīng)基本類型與氧化還原反應(yīng)之間的關(guān)系��。
(3)認(rèn)識物質(zhì)的量及其單位——摩爾的含義��。
(4)理解物質(zhì)的量��、物質(zhì)的粒子數(shù)��、物質(zhì)的質(zhì)量��、摩爾質(zhì)量之間的聯(lián)系��,能根據(jù)它們之間的關(guān)系進(jìn)行簡單計算��。
(5)理解用化學(xué)方程式表示反應(yīng)物和生成物之間物質(zhì)的量的關(guān)系��。
(6)知道不同聚集狀態(tài)物質(zhì)的一些特性��,根據(jù)物質(zhì)的存在狀態(tài)進(jìn)行分類��,知道固��、液��、氣態(tài)物質(zhì)的一些特性��。
(7)了解影響氣體體積的主要因素��,初步學(xué)會運用氣體摩爾體積等概念進(jìn)行簡單的計算��。
(8)了解分散系的含義��,知道膠體區(qū)別于其他分散系的本質(zhì)特征和鑒別方法��。
(9)知道膠體是一種常見的分散系��,了解膠
8、體的重要性質(zhì)和應(yīng)用��。
(10)知道電解質(zhì)和非電解質(zhì)��,初步學(xué)會書寫離子方程式��。
三��、重難點分析
教材對難點進(jìn)行了分散安排��,將某些概念安排在不同模塊中逐步深化��,這種設(shè)置方式符合學(xué)生認(rèn)識水平螺旋式發(fā)展的特點��,有效地方病保護(hù)了學(xué)生學(xué)習(xí)化學(xué)的積極性��。因此在教學(xué)中不宜采取一步到位的方法��。
1.對氧化還原反應(yīng)只要求學(xué)會判斷��,如果學(xué)生在初中沒有學(xué)習(xí)依據(jù)得失氧來判斷氧化還原反應(yīng)��,不必特意增加這個判斷依據(jù)��。不要對其它概念(氧化反應(yīng)、還原反應(yīng)��、氧化劑��、還原劑等)進(jìn)行擴(kuò)展��,也不對復(fù)雜氧化還原反應(yīng)進(jìn)行配平��。相關(guān)內(nèi)容將在后續(xù)課程中學(xué)習(xí)��。
2.物質(zhì)的量是本單元的重難點��,但在教學(xué)中不應(yīng)對學(xué)生過多的強(qiáng)調(diào)其重要性��,以
9��、免引起學(xué)生的恐懼心理��,重點在于知道物質(zhì)的量是基本物理量��,并能利用物質(zhì)的量進(jìn)行簡單計算��。不宜在概念上過多糾纏��。
3.氣體摩爾體積的教學(xué)重點在于能進(jìn)行簡單計算��,阿伏加德羅定律的推論不作要求��。
4.對晶體和非晶體的結(jié)構(gòu)特點和性質(zhì)差異只作簡單介紹��,或作為課外閱讀材料��。
5.能判斷電解質(zhì)和非電解質(zhì)��,并書寫常見物質(zhì)的電離方程式��,但不要求區(qū)別強(qiáng)弱電解質(zhì)��,更不宜涉及離子反應(yīng)等內(nèi)容��。
6.膠體的概念只要求了解其不同于溶液的特性��,對膠體的凝聚��、布朗運動等不宜擴(kuò)展��。
四��、實驗研究
1.在演示氣溶膠的丁達(dá)爾現(xiàn)象時��,向一錐形瓶中滴入幾滴濃氨水��,用玻璃棒蘸取濃鹽酸伸入錐形瓶中,使之形成煙即氣溶膠��,讓激光柱
10��、通過錐形瓶��,對這些再進(jìn)行實物投影��,展現(xiàn)于銀幕��。激光是紅色的��,通過白煙時的現(xiàn)象非常美麗��。
2.氫氧化鐵膠體溶液的制備��,為了操作上的方便與快速��,在20mL煮沸的蒸餾水中加入2 ~3滴FeCl3飽和溶液��,便得到清澈透明的紅褐色Fe(OH)3膠體��,加入FeCl3的量不宜多��,否則將生成Fe(OH)3沉淀��。
3.如果要增加明礬的凈水實驗��,可以用這樣的配比:200mL渾濁的水中滴加10滴(0.5mL)飽和明礬溶液即可以達(dá)到理想的潔凈效果��。如果所加明礬太多��,酸度將增大��,Al(OH)3膠體的量就不會很多��,潔凈水的效果反倒不好��。
五��、教學(xué)建議
1.教材有豐富多彩的欄目設(shè)置��,蘊(yùn)涵著教與學(xué)的方法��,體現(xiàn)了新課程
11��、的理念��,能夠充分調(diào)動教師教與學(xué)生學(xué)的積極性��,教師可以充分開發(fā)利用教材資源��。
2.整個單元的教學(xué)設(shè)計要圍繞“物質(zhì)”中心,從物質(zhì)的分類��、變化到物質(zhì)的處理(分離��、提純及檢驗)再到物質(zhì)內(nèi)在結(jié)構(gòu)的研究��,從而使學(xué)生對“物質(zhì)”的整體知識有較為全面的了解��。
3.精心創(chuàng)設(shè)多種問題情景:可來源于生活經(jīng)驗��,如物質(zhì)聚集狀態(tài)��,同位素的應(yīng)用��;來源于生產(chǎn)實際��,如自然界中存在的晶體��;來源于學(xué)生的學(xué)習(xí)��,如對已有原子結(jié)構(gòu)的認(rèn)識��;來源于科學(xué)史料��,如原子結(jié)構(gòu)模型的演變��,無機(jī)化合物轉(zhuǎn)變?yōu)橛袡C(jī)化合物的史料��。舉例要適當(dāng)��、典型��,不宜選用學(xué)生不太熟悉的反應(yīng)實例��。注意與初中自然學(xué)科相關(guān)知識的銜接��,確保學(xué)生的可接受性��。
4.物質(zhì)的量概念中包含著微觀粒子的計量方法��,氣體摩爾體積中包含著氣體物質(zhì)的計量方法��,物質(zhì)的量和氣體摩爾體積等概念中還包含著有關(guān)化學(xué)計算的技能��。教學(xué)設(shè)計中要注意這方面知識和技能目標(biāo)的把握��。
5.氣體摩爾體積教學(xué)中��,要充分運用實物��、圖片��、實例進(jìn)行分析,使學(xué)生理解學(xué)習(xí)氣體摩爾體積的意義��。并能進(jìn)行簡單的計算��。
6.在教學(xué)中要注意階段學(xué)習(xí)目標(biāo)的達(dá)成��,嚴(yán)格控制教學(xué)深度��、難度��,避免學(xué)生在剛開始高中化學(xué)學(xué)習(xí)的時候就產(chǎn)生畏難情緒��。
 2022年高中化學(xué) 《豐富多彩的化學(xué)物質(zhì)》教案1 蘇教版必修1
2022年高中化學(xué) 《豐富多彩的化學(xué)物質(zhì)》教案1 蘇教版必修1