《新編高二化學(xué)蘇教版選修四作業(yè):專題1 第2單元第2課時(shí) 電解池的工作原理及應(yīng)用》由會員分享�����,可在線閱讀����,更多相關(guān)《新編高二化學(xué)蘇教版選修四作業(yè):專題1 第2單元第2課時(shí) 電解池的工作原理及應(yīng)用(3頁珍藏版)》請?jiān)谘b配圖網(wǎng)上搜索���。
1�、新編化學(xué)精品資料
化學(xué)反應(yīng)原理》專題一 化學(xué)反應(yīng)與能量變化
專題一第二單元化學(xué)能與電能的轉(zhuǎn)化
電解池的工作原理及應(yīng)用
1.在原電池和電解池的電極上所發(fā)生的反應(yīng)���,同屬氧化反應(yīng)或同屬還原反應(yīng)的是 ( ) A.原電池的正極和電解池的陽極所發(fā)生的反應(yīng)( BC )
B.原電池的正極和電解池的陰極所發(fā)生的反應(yīng)
C.原電池的負(fù)極和電解池的陽極所發(fā)生的反應(yīng)
D.原電池的負(fù)極和電解池的陰極所發(fā)生的反應(yīng)
2.在鐵制品上鍍一定厚度的鋅層����,以下方案設(shè)計(jì)正確的是 ( )
2���、
A.鋅做陽極�,鍍件做陰極�,溶液中含有鋅離子
B.鉑做陰極,鍍件做陽極���,溶液中含有鋅離子
C.鐵做陽極����,鍍件做陰極�����,溶液中含有亞鐵離子
D.鋅做陰極���,鍍件做陽極�,溶液中含有鋅離子
3.用鉑電極電解CuSO4溶液,當(dāng)Cu2+濃度降低至原來一半時(shí)停止通電�����,若加入下列物質(zhì)能使溶液恢復(fù)成原來成分和濃度的是 ( )B
A.無水CuSO4 B.CuO C.Cu(OH)2 D.CuSO4·5H2O
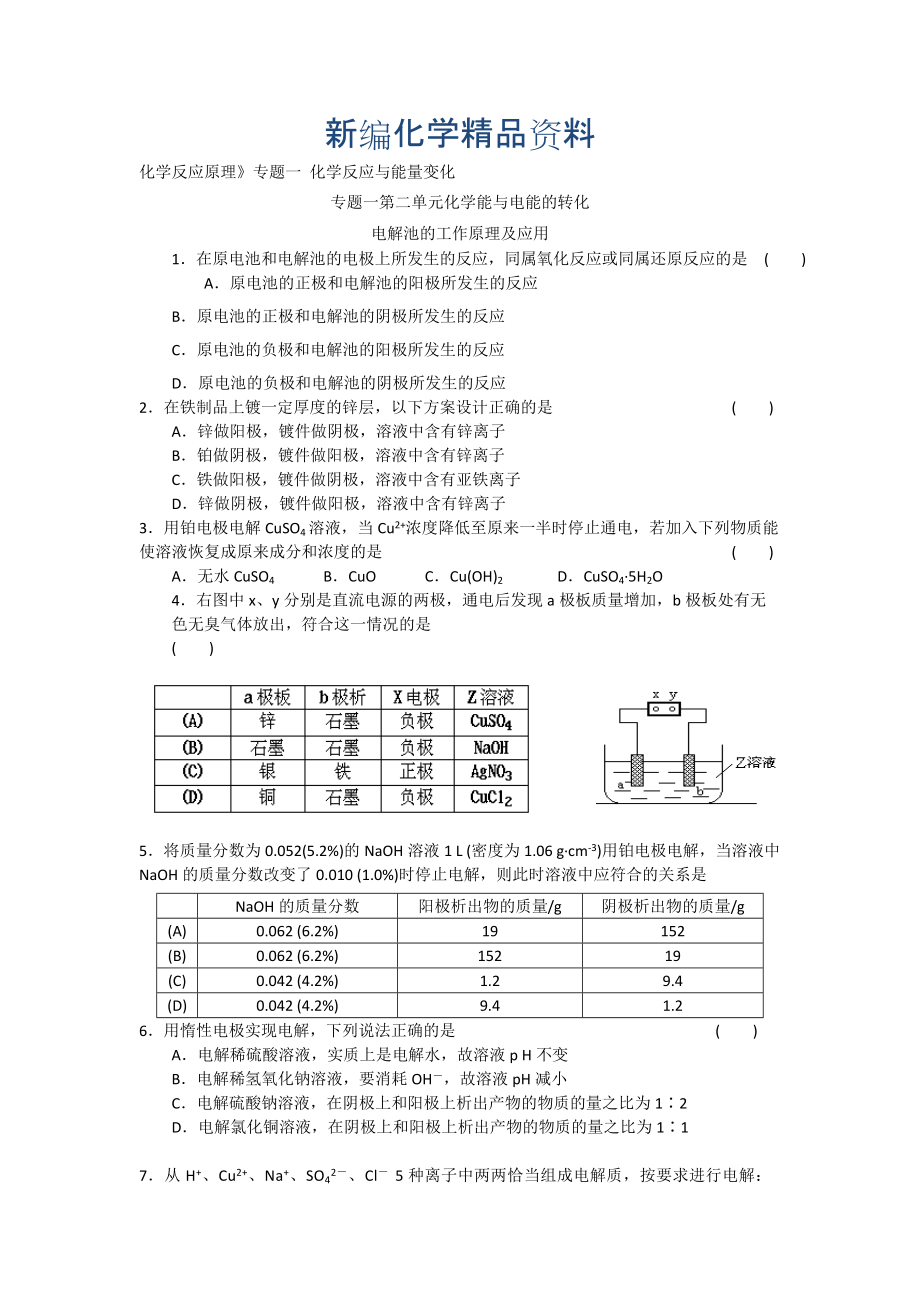
4.右圖中x�、y分別
3、是直流電源的兩極�,通電后發(fā)現(xiàn)a極板質(zhì)量增加,b極板處有無色無臭氣體放出���,符合這一情況的是 ( )
5.將質(zhì)量分?jǐn)?shù)為0.052(5.2%)的NaOH溶液1 L (密度為1.06 g·cm-3)用鉑電極電解�,當(dāng)溶液中NaOH的質(zhì)量分?jǐn)?shù)改變了0.010 (1.0%)時(shí)停止電解�,則此時(shí)溶液中應(yīng)符合的關(guān)系是B
NaOH的質(zhì)量分?jǐn)?shù)
陽極析出物的質(zhì)量/g
陰極析出物的質(zhì)量/g
(A)
0.062 (6.2%)
19
152
(B)
0.062 (6.2%)
4、
152
19
(C)
0.042 (4.2%)
1.2
9.4
(D)
0.042 (4.2%)
9.4
1.2
6.用惰性電極實(shí)現(xiàn)電解�,下列說法正確的是 ( )(D)
A.電解稀硫酸溶液,實(shí)質(zhì)上是電解水�,故溶液p H不變
B.電解稀氫氧化鈉溶液,要消耗OH-�,故溶液pH減小
C.電解硫酸鈉溶液,在陰極上和陽極上析出產(chǎn)物的物質(zhì)的量之比為1∶2
D.電解氯化銅溶液����,在陰極上和陽極上析出產(chǎn)物的物質(zhì)的量之比為1∶1
7.從H+、Cu2+�、Na+����、SO42-����、Cl- 5種離子中兩兩恰當(dāng)組成電解質(zhì)�,
5、按要求進(jìn)行電解:
(1)以碳棒為電極,使電解質(zhì)質(zhì)量減少,水量不變進(jìn)行電解���,則采用的電解質(zhì)是 ���;
(2)以碳棒為電極,使電解質(zhì)質(zhì)量不變,水量減少進(jìn)行電解,則采用的電解質(zhì)是 �����;
(3)以鉑為電極,使電解質(zhì)和水量都減少進(jìn)行電解���,則電解質(zhì)是 �。
A
X
Y
+
―
8.電解原理在化學(xué)工業(yè)中有廣泛應(yīng)用����。右圖表示一個(gè)電解池�,裝有電解液a���;X�����、Y是兩塊電極板�����,通過導(dǎo)線與直流電源相連�。請回答以下問題:
(1)若X�����、Y都是惰性電極�����,a是飽和NaCl溶液�,實(shí)驗(yàn)開始時(shí),
同時(shí)在兩邊各滴入幾滴酚酞
6���、試液�,則電解池中X極上的電極反
應(yīng)式為 ,在X極附近觀察到的實(shí)驗(yàn)現(xiàn)象
是 ���,Y電極上的電極反應(yīng)式為 ���,
a
a
檢驗(yàn)該電極反應(yīng)產(chǎn)物的方法是 ?����!?
(2)如要用電解方法精煉粗銅�����,電解液a選用CuSO4溶液�����,則
①X電極的材料是 ����,電極反應(yīng)式為 ���。
②Y電極的材料是 ����,電極反應(yīng)式為 。
9.含Cr
7���、2O72-的工業(yè)酸性廢水會造成鉻污染����,排放前要進(jìn)行如下處理:(Ⅰ)往工業(yè)廢水中加入適量的NaCl攪拌均勻�����;(Ⅱ)以Fe做兩電極進(jìn)行電解�,從而使溶液的pH不斷升高,廢水由酸性轉(zhuǎn)化為堿性����,經(jīng)過一段時(shí)間有Cr(OH)3和Fe(OH)3沉淀產(chǎn)生:(Ⅲ)過濾回收沉淀,廢水達(dá)到排放標(biāo)準(zhǔn)�����。
(1)在電解過程中����,溶液pH不斷升高的原因可能是 ( )
①電解時(shí)廢水的體積不斷減小 ②電解時(shí)H+在陰極被還原 ③作為陽極的Fe不斷溶解 ④Cr2O72-轉(zhuǎn)化為Cr3+時(shí)消耗了H+ ⑤NaCl在電解時(shí)轉(zhuǎn)化成了NaOH
A.⑤ B.②④ C.②③④
8�、 D.①②③④
(2)兩極發(fā)生反應(yīng)的電極反應(yīng)式為:
陽極:
陰極:
(3)寫出Cr2O72-變成Cr3+的離子方程式__________________________________���。
(4)_________(填“能”或“不能”)改用石墨電極進(jìn)行電解����。
10.我國缺碘病區(qū)甚廣���,防治缺碘病的主要措施是食鹽中加碘�。1996年我國政府以國家標(biāo)準(zhǔn)的方式規(guī)定食鹽的碘添加劑是KIO
9�、3。
(1)可用鹽酸酸化的KI和淀粉的混合物檢驗(yàn)食鹽是否為加碘鹽�����,反應(yīng)的化學(xué)方程式為__________________________________ �����。
(2)可用電化學(xué)方法制備KIO3���。原理是:以石墨為陽極,不銹鋼為陰極�����,以KI溶液(加入少量K2Cr2O7)為電解質(zhì)溶液,在一定電流強(qiáng)度和溫度下進(jìn)行電解���,其電解總反應(yīng)方程式為KI+3H2OKIO3+3H2↑�。試寫出兩極反應(yīng)式:陽極_____________ �����;
陰極_____________ �����。
(3)如果在容積為10 L的離子交換膜電解槽中���,1 min時(shí)陰極可產(chǎn)生11.2 L(標(biāo)準(zhǔn)狀況)Cl2�����,這時(shí)溶液的c(H+)是(設(shè)體積維持不變)_____________���。
(4)Cl2常用于自來水的消毒殺菌,現(xiàn)有一種新型消毒劑ClO2,若它們在殺菌過程中的還原產(chǎn)物均為Cl-�����,消毒等量的自來水����,所需Cl2和ClO2的物質(zhì)的量之比為_____________。
 新編高二化學(xué)蘇教版選修四作業(yè):專題1 第2單元第2課時(shí) 電解池的工作原理及應(yīng)用
新編高二化學(xué)蘇教版選修四作業(yè):專題1 第2單元第2課時(shí) 電解池的工作原理及應(yīng)用