《2022-2023學年高中化學(期末復習備考)每日一題 化學反應速率大小的比較(含解析)新人教版選修4》由會員分享�,可在線閱讀,更多相關(guān)《2022-2023學年高中化學(期末復習備考)每日一題 化學反應速率大小的比較(含解析)新人教版選修4(6頁珍藏版)》請在裝配圖網(wǎng)上搜索�。
1、2022-2023學年高中化學(期末復習備考)每日一題 化學反應速率大小的比較(含解析)新人教版選修4
化合物AX3和單質(zhì)X2在一定條件下反應可生成化合物AX5�。回答下列問題:
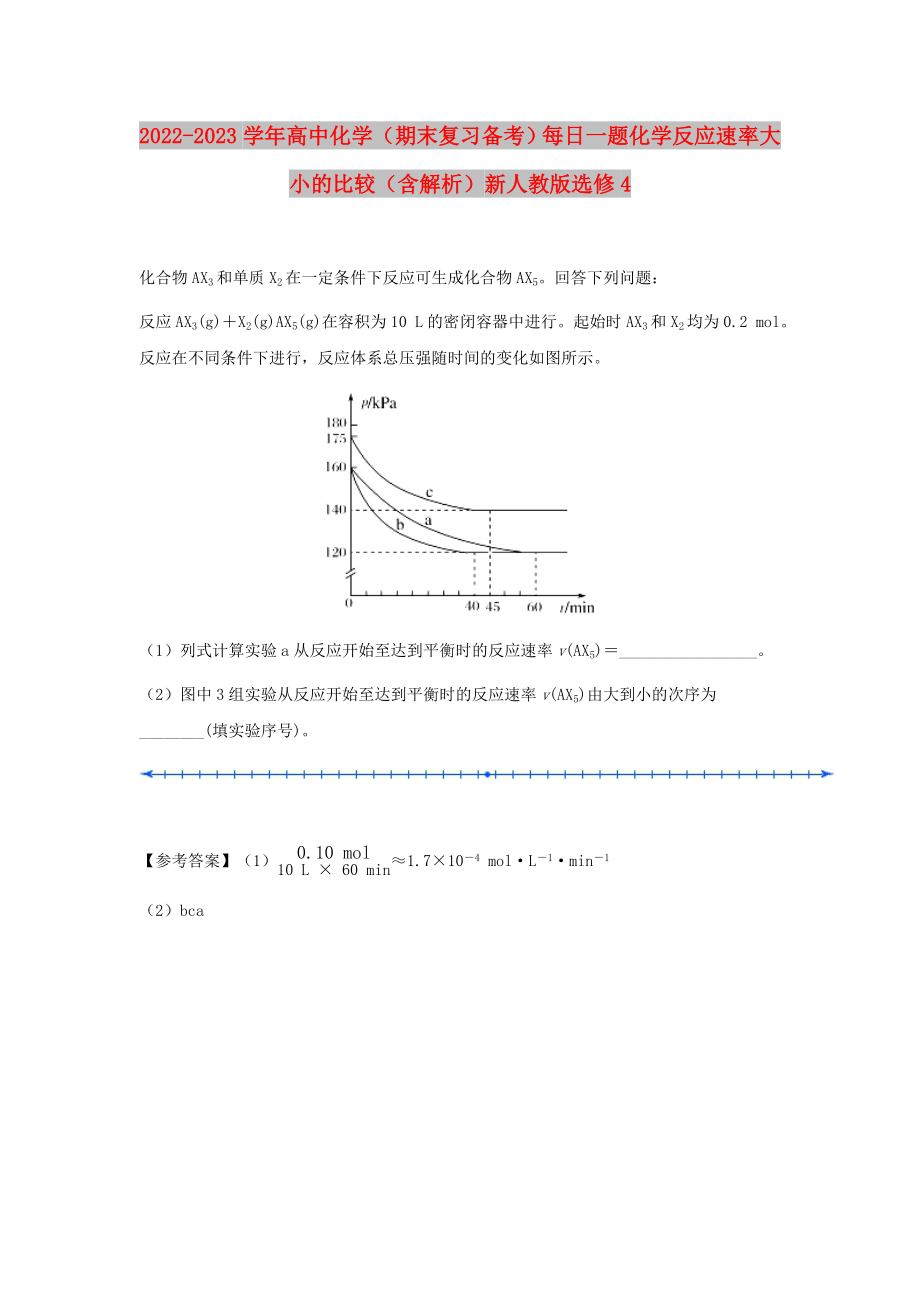
反應AX3(g)+X2(g)AX5(g)在容積為10 L的密閉容器中進行�。起始時AX3和X2均為0.2 mol。反應在不同條件下進行�,反應體系總壓強隨時間的變化如圖所示。
(1)列式計算實驗a從反應開始至達到平衡時的反應速率v(AX5)=_________________�。
(2)圖中3組實驗從反應開始至達到平衡時的反應速率v(AX5)由大到小的次序為________(填實驗序號)。
【參考
2�、答案】(1)10 L×60 min(0.10 mol)≈1.7×10-4 mol·L-1·min-1
(2)bca
(2)由(1)可知到達平衡時生成AX5的量為0.10 mol。實驗b從反應開始至達到平衡時所用時間為40 min�,其反應速率v(AX5)=10 L×40 min(0.10 mol)=2.5×10-4 mol·L-1·min-1。實驗c達到平衡時氣體總物質(zhì)的量n=0.40 mol×175 kPa(140 kPa)=0.32 mol�,從反應開始到達到平衡時的反應速率v(AX5)=10 L×45 min(0.08 mol)≈1.8×10-4 mol·L-1·min-1。所以v
3�、(AX5)由大到小的順序是bca�。
比較化學反應速率大小的三步驟
(1)變換單位——將各反應速率的單位統(tǒng)一�。
(2)轉(zhuǎn)換物質(zhì)——將各反應速率轉(zhuǎn)換成用同一物質(zhì)表示的反應速率(一般轉(zhuǎn)換成化學計量數(shù)最小的物質(zhì))。
(3)比較大小——比較各反應速率的數(shù)值大小�。
1.在四個不同的容器中,在不同條件下進行合成氨反應�。根據(jù)下列在相同時間內(nèi)測定的結(jié)果判斷生成氨的速率最快的是
A.v(H2)=0.1 mol·(L·min)?1 B.v(N2)=0.1 mol·(L·min)?1
C.v(N2)=0.2 mol·(L·min)?1 D.v(NH3)=0.3 mol·(
4、L·s)?1
2.反應A(g)+3B(g)===2C(g)+2D(g)在四種不同情況下的反應速率分別為①v(A)=0.45 mol·L-1·s-1②v(B)=0.6 mol·L-1·s-1 ③v(C)=0.4 mol·L-1·s-1 ④v(D)=0.45 mol·L-1·s-1�。
下列有關(guān)反應速率的比較中正確的是
A.④>③=②>① B.①>④>②=③
C.①>②>③>④ D.④>③>②>①
3.某學生用純凈的Cu與過量濃HNO3反應制取NO2,實驗結(jié)果如圖所示�,對圖中曲線的描述正確的是
A.OA段表示開始時,反應速率稍慢
B.AB段表示反應速率較快�,可能因為產(chǎn)物有
5、催化作用
C.BC段表示反應速率最快�,在該時間內(nèi)收集到的氣體最多
D.OC線表示隨時間增加,反應速率逐漸增大
4.一定溫度下�,10 mL 0.40 mol·L-1 H2O2溶液發(fā)生催化分解。不同時刻測得生成O2的體積(已折算為標準狀況)如下表:
t/min
0
2
4
6
8
10
V(O2)/mL
0.0
9.9
17.2
22.4
26.5
29.9
下列敘述不正確的是(溶液體積變化忽略不計)
A.0~6 min的平均反應速率:v(H2O2)≈3.3×10-2 mol·(L·min)-1
B.6~10 min的平均反應速率:v(H2O2)<3.3×1
6�、0-2 mol·(L·min)-1
C.反應至6 min時,c(H2O2)=0.30 mol·L-1
D.反應至6 min時�,H2O2分解了50%
5.一定溫度下,向容積為2 L的密閉容器中通入兩種氣體發(fā)生化學反應�,生成的產(chǎn)物也是氣體,反應中各物質(zhì)的物質(zhì)的量變化如圖所示�。請回答下列問題:
(1)反應進行到6 s時,B的平均反應速率為_____________�。
(2)該反應的化學方程式為__________________�。
(3)若該反應分別在甲�、乙、丙�、丁四個相同的密閉容器中進行�,經(jīng)相同的一段時間后,測得四個容器中的反應速率分別為
甲:v(A)=0.75 mol·L?1
7�、·min?1
乙:v(B)=0.01 mol·L?1·s?1
丙:v(C)=0.40 mol·L?1·min?1
丁:v(D)=0.45 mol·L?1·min?1
則甲�、乙、丙�、丁四個容器中反應速率由大到小的順序為_____________________。
1.【答案】D
【解析】本題考查化學反應速率的計算與大小比較�。合成氨的化學方程式為N2(g)+3H2(g)2NH3(g),根據(jù)速率比等于化學計量數(shù)之比�,把四個選項的速率換算成用N2表示的速率,則A.v(N2)=v(H2)=0.03 mol·(L·min)?1�;D.v(N2)=v(NH3)=0.15 mol·(L·s)?
8、1=9 mol·(L·min)?1�。答案選D。
2.【答案】B
【解析】用比值法進行反應速率大小的比較�,v(A)=0.45 mol·L-1·s-1;3(1)v(B)=3(1)×0.6=0.2(mol·L-1·s-1)�;2(1)v(C)=2(1)×0.4=0.2(mol·L-1·s-1);2(1)v(D)=2(1)×0.45=0.225(mol·L-1·s-1)�,故①>④>②=③�,B項正確�。
3.【答案】A
4.【答案】C
【解析】根據(jù)題目信息可知,0~6 min�,生成22.4 mL(標準狀況)氧氣,消耗0.002 mol H2O2�,則v(H2O2)≈3.3×10-2 mol·(
9、L·min)-1�,A項正確;隨反應物濃度的減小�,反應速率逐漸降低,B項正確�;反應至6 min時,剩余0.002 mol H2O2�,此時c(H2O2)=0.20 mol·L-1,C項錯誤�;反應至6 min時,消耗0.002 mol H2O2�,轉(zhuǎn)化率為50%,D項正確�。
5.【答案】(1)0.05 mol·L?1·s?1
(2)3B(g)+4C(g)6A(g)+2D(g)
(3)丁>乙>甲>丙
【解析】(1)v(B)===0.05 mol·L?1·s?1。
(2)圖中各物質(zhì)的物質(zhì)的量變化之比等于化學方程式中化學計量數(shù)之比�,Δn(A)∶Δn(B)∶Δn(C)∶Δn(D)=(1.2?0)mo
10、l∶(1.0?0.4) mol∶(1.0?0.2) mol∶(0.4?0) mol=6∶3∶4∶2�,所以反應的化學方程式為3B(g)+4C(g)6A(g)+2D(g)。
(3)根據(jù)v(A)∶v(B)∶v(C)∶v(D)=6∶3∶4∶2�,轉(zhuǎn)化為用B的濃度變化表示的反應速率�,甲容器中v(B)=0.75/2 mol·L?1·min?1=0.375 mol·L?1·min?1�;乙容器中v(B)=0.60 mol·L?1·min?1;丙容器中v(B)= 0.40 mol·L?1·min?1×=0.30 mol·L?1·min?1�;丁容器中v(B)=0.45 mol·L?1·min?1×=0
11、.675 mol·L?1·min?1�。故甲、乙�、丙、丁四個容器中反應速率由大到小的順序為丁>乙>甲>丙�。
你正走在學霸的路上�!
_________________________________________________________________________________________
_________________________________________________________________________________________
______________________________
12、___________________________________________________________
_________________________________________________________________________________________
_________________________________________________________________________________________
_________________________________________________________
13�、________________________________
金創(chuàng)神藥
魔術(shù)演示:魔術(shù)師對觀眾說:“我有一種金創(chuàng)神藥,外傷出血敷上立竿見影�,不但止血止痛,而且會讓皮膚完好如初�。”魔術(shù)師拿出醫(yī)用碘酊和棉簽�,用棉簽蘸碘酊在左臂上擦幾下,接著�,又拿出一把小刀,將小刀浸入燒杯里的水中�,簡單清洗一下。清洗完之后�,魔術(shù)師用右手執(zhí)刀�,用力向左臂切去�,左臂傷口流出鮮血。這時�,魔術(shù)師用右手急忙將一些白色的藥粉敷在傷口上,然后用右手指壓住�。兩分鐘之后,魔術(shù)師拿開右手�,左臂上的傷口已經(jīng)不見了,皮膚完好如初�!
魔術(shù)揭秘:在表演節(jié)目之前,魔術(shù)師用堿面和清水勾兌成堿水備用�。然后準備少許中藥大黃,放入坩堝�,加入清水,讓水沒過大黃�。浸泡十幾分鐘之后,點燃酒精燈�,將坩堝放在酒精燈上加熱。等到坩堝里剩下少許濃藥汁的時候�,熄滅酒精燈。找一個干凈的碘酊空瓶�,把大黃汁裝進去,擰好瓶蓋�。表演的時候,對觀眾說瓶子里裝的是碘酊,可以用它來消毒�。魔術(shù)師在表演時假裝清洗一下小刀,其實是讓小刀浸入堿水里�。把大黃熬汁擦在皮膚上,用在堿水浸過的刀切皮膚�,刀刃和皮膚接觸,就會在皮膚上出現(xiàn)殷紅的液體�,就像是傷口在流血,其實是大黃藥汁和堿溶液發(fā)生化學反應�,生成紅色液體。至于用的白色藥粉�,其實是感冒膠囊里面的藥粉,沒有任何秘密�。
 2022-2023學年高中化學(期末復習備考)每日一題 化學反應速率大小的比較(含解析)新人教版選修4
2022-2023學年高中化學(期末復習備考)每日一題 化學反應速率大小的比較(含解析)新人教版選修4